Rappels sur la dissolution
et sur la dilution.
Une solution est un mélange homogène d’un soluté dans un solvant.
Ex : sucre dans l’eau, café dans le lait.
Dissolution
Une dissolution est l’opération consistant à obtenir une solution homogène en mélangeant un soluté à un solvant.
Le soluté est l’espèce dissoute dans un solvant, constituant minoritaire d’une solution. Le solvant est le constituant principal d’une solution.
Une solution possède une concentration massique, ou titre massique. On peut aussi utiliser la concentration molaire.
|
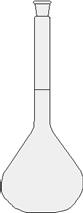
Verrerie : une dissolution a lieu dans une fiole jaugée. On place le soluté, puis on ajuste le solvant jusqu’au trait de jauge. On agite jusqu’à dissolution complète. |
|
|
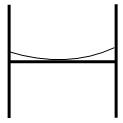
Rem : le bas du ménisque doit toujours être tangent au trait de jauge. |
|
Dilution
Lorsque l’on veut diminuer la concentration d’une solution, on ajoute du solvant : c’est la dilution.
Ex : un sirop de menthe trop sucré, on ajoute de l’eau (qui est le solvant) pour le diluer.
Lors d’une dilution, on passe d’une solution mère (appelée S0, de concentration c0) à une solution fille moins concentrée (appelée S1, de concentration c1) et dont on fixe le volume que l’on veut fabriquer, v1.
On appelle facteur de dilution le rapport entre c0
et c1, ![]() ,
qui signifie combien de fois la solution fille sera moins diluée que la
solution mère.
,
qui signifie combien de fois la solution fille sera moins diluée que la
solution mère.
Première méthode :
pour diluer k fois, il faut prélever un volume de solution mère k fois plus
petit que le volume de solution fille désiré, ![]() .
.
Deuxième méthode :
on a la relation mathématique c0xv0 = c1xv1,
qui s’écrit aussi ![]()
Exemples :
1) On veut fabriquer 50 mL d’une solution aqueuse de sel de concentration massique 2 g/L à partir d’une solution mère de concentration massique 10 g/L. Quel volume de solution mère utiliser ?
2) On part d’une solution mère S0 de concentration c0 = 3,0 g.L-1, on en prélève un volume de 20 mL. On place ces 20 mL dans une fiole jaugée de 250 mL et on complète jusqu’au trait de jauge avec de l’eau distillée. On bouche et on homogénéise soigneusement. Quelle est la concentration de la solution fille c1 obtenue ?
Réponses :
1) On veut diluer 5 fois (passer de 10 g/L à 2 g/L, 10/2 = 5). Comme le volume de solution fille désiré est de 50 mL, il faut prélever 50/5 = 10 mL de solution mère.
2) Comme on passe d’un volume de 20 mL à un volume de 250 mL, le soluté est contenu à la fin dans un volume 250 / 20 = 12,5 fois plus grand. Donc la concentration est 12,5 fois plus petite, ce qui donne c1 = c0 / 12,5 = 3,0 / 12,5 = 0,24 g.L-1.
Verrerie :
|
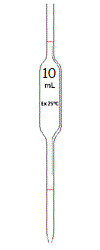
-pour la solution mère : si le volume est rond (5, 10, 20 mL), une pipette jaugée. |
|
|
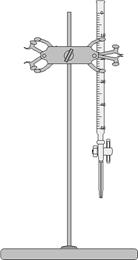
-pour la solution mère : si le volume est quelconque : une pipette graduée ou une burette graduée. |
|
|
-pour la solution fille : une fiole jaugée. |
|
Rem : ne pas oublier d’homogénéiser.